Электрохимический ряд напряжений
Разность потенциалов «вещество электрода – раствор» как раз и служит количественной характеристикой способности вещества (как металлов, так и неметаллов) переходить в раствор в виде ионов, т.е. характеристикой ОВ способности иона и соответствующего ему вещества.
Такую разность потенциалов называют электродным потенциалом.
Однако прямых методов измерений такой разности потенциалов не существует, поэтому условились их определять по отношению к так называемому стандартному водородному электроду, потенциал которого условно принят за ноль (часто его также называют электродом сравнения). Стандартный водородный электрод состоит из платиновой пластинки, погруженной в раствор кислоты с концентрацией ионов Н+ 1 моль/л и омываемой струей газообразного водорода при стандартных условиях 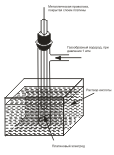 .
.
Возникновение потенциала на стандартном водородном электроде можно представить себе следующим образом. Газообразный водород, адсорбируясь платиной, переходит в атомарное состояние:
H2 ![]() 2H.
2H.
Между атомарным водородом, образующимся на поверхности пластины, ионами водорода в растворе и платиной (электроны!) реализуется состояние динамического равновесия:
H![]() Н+ + е.
Н+ + е.
Суммарный процесс выражается уравнением:
Н2 ![]() 2Н+ + 2е.
2Н+ + 2е.
Платина не принимает участия в окислительно — восстановительном процессе, а является лишь носителем атомарного водорода.
Если пластинку некоторого металла, погруженную в раствор его соли с концентрацией ионов металла, равной 1 моль/л, соединить со стандартным водородным электродом, то получится гальванический элемент. Электродвижущая сила этого элемента (ЭДС), измеренная при 25° С, и характеризует стандартный электродный потенциал металла, обозначаемый обычно как Е0.
По отношению к системе Н2/2Н+ некоторые вещества будут вести себя как окислители, другие — как восстановители. В настоящее время получены стандартные потенциалы практически всех металлов и многих неметаллов, которые характеризуют относительную способность восстановителей или окислителей к отдаче или захвату электронов.
Потенциалы электродов, выступающих как восстановители по отношению к водороду, имеют знак “-“, а знаком “+” отмечены потенциалы электродов, являющихся окислителями.
Если расположить металлы в порядке возрастания их стандартных электродных потенциалов, то образуется так называемый электрохимический ряд напряжений металлов:
Li, Rb, К, Ва, Sr, Са, Nа, Мg, Аl, Мn, Zn, Сr, Fе, Сd, Со, Ni, Sn, Рb, Н, Sb, Вi, Сu, Hg, Аg, Рd, Рt, Аu.
Ряд напряжений характеризует химические свойства металлов.
1. Чем более отрицателен электродный потенциал металла, тем больше его восстановительная способность.
2. Каждый металл способен вытеснять (восстанавливать) из растворов солей те металлы, которые стоят в ряду напряжений металлов после него. Исключениями являются лишь щелочные и щелочноземельные металлы, которые не будут восстанавливать ионы других металлов из растворов их солей. Это связано с тем, что в этих случаях с большей скоростью протекают реакции взаимодействия металлов с водой.
3. Все металлы, имеющие отрицательный стандартный электродный потенциал, т.е. находящиеся в ряду напряжений металлов левее водорода, способны вытеснять его из растворов кислот.
Необходимо отметить, что представленный ряд характеризует поведение металлов и их солей только в водных растворах, поскольку потенциалы учитывают особенности взаимодействия того или иного иона с молекулами растворителя. Именно поэтому электрохимический ряд начинается литием, тогда как более активные в химическом отношении рубидий и калий находятся правее лития. Это связано с исключительно высокой энергией процесса гидратации ионов лития по сравнению с ионами других щелочных металлов.
Алгебраическое значение стандартного окислительно-восстановительного потенциала характеризует окислительную активность соответствующей окисленной формы. Поэтому сопоставление значений стандартных окислительно-восстановительных потенциалов позволяет ответить на вопрос: протекает ли та или иная окислительно-восстановительная реакция?
Так, все полуреакции окисления галогенид-ионов до свободных галогенов
2Cl—— 2e = Сl2 Е0= -1,36 В (1)
2Br—-2е = Вr2 E0 = -1,07 В (2)
2I—-2е = I2 E0 = -0,54 В (3)
могут быть реализованы в стандартных условиях при использовании в качестве окислителя оксида свинца (IV) (Е0 = 1,46 В) или перманганата калия (Е0 = 1,52 В). При использовании дихромата калия (E0 = 1,35 В) удается осуществить только реакции (2) и (3). Наконец, использование в качестве окислителя азотной кислоты (E0 = 0,96 В) позволяет осуществить только полуреакцию с участием иодид-ионов (3).
Таким образом, количественным критерием оценки возможности протекания той или иной окислительно-восстановительной реакции является положительное значение разности стандартных окислительно-восстановительных потенциалов полуреакций окисления и восстановления.
