Синтезы для выработки антибиотика
Новая стратегия получения природного соединения также может быть использована для создания вариантов с еще более сильным антимикробным действием.
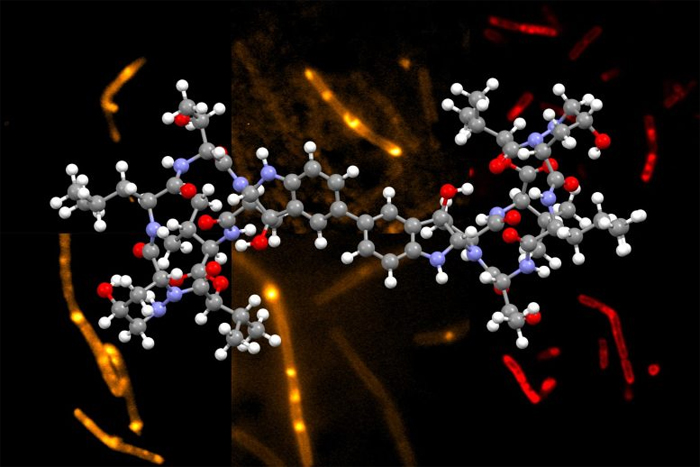
Химики Массачусетского технологического института разработали новый способ синтеза гимастатина, сложной природной молекулы, которая может иметь потенциал в качестве антибиотика. Кредит: Предоставлено исследователями.
Химики Массачусетского технологического института разработали новый способ синтеза гимастатина, природного соединения, которое показало потенциал в качестве антибиотика.
Используя свой новый синтез, исследователи смогли не только произвести гимастатин, но и создать варианты молекулы, некоторые из которых также проявляли противомикробную активность. Они также обнаружили, что это соединение убивает бактерии, разрушая их клеточные мембраны. Теперь исследователи надеются разработать другие молекулы, которые могли бы обладать еще более сильной антибиотической активностью.
«Что мы хотим сделать прямо сейчас, так это изучить молекулярные детали того, как это работает, чтобы мы могли разработать структурные мотивы, которые могли бы лучше поддерживать этот механизм действия. Сейчас мы прилагаем большие усилия, чтобы узнать больше о физико-химических свойствах этой молекулы и о том, как она взаимодействует с мембраной», — говорит Мохаммад Мовассаги, профессор химии Массачусетского технологического института и один из ведущих авторов исследования.
Брэд Пентелюте, профессор химии Массачусетского технологического института, также является старшим автором исследования, которое было опубликовано 24 февраля 2022 года в журнале Science . Выпускник Массачусетского технологического института Киан Д’Анджело является ведущим автором исследования, а аспирантка Карли Шиссел также является автором.
Подражание природе
Гимастатин, продуцируемый одним из видов почвенных бактерий, был впервые обнаружен в 1990-х годах. В исследованиях на животных было обнаружено, что он обладает противораковой активностью, но необходимые дозы имели токсические побочные эффекты. Соединение также показало потенциальную противомикробную активность, но этот потенциал подробно не изучался, говорит Мовассаги.
Химастатин представляет собой сложную молекулу, состоящую из двух идентичных субъединиц, известных как мономеры, которые соединяются вместе, образуя димер. Две субъединицы связаны вместе связью, которая соединяет шестиуглеродное кольцо в одном из мономеров с идентичным кольцом в другом мономере.
Эта углерод-углеродная связь имеет решающее значение для антимикробной активности молекулы. В предыдущих попытках синтезировать гимастатин исследователи пытались сначала создать эту связь, используя две простые субъединицы, а затем добавляя к мономерам более сложные химические группы.
Команда Массачусетского технологического института применила другой подход, вдохновленный тем, как эта реакция протекает у бактерий, вырабатывающих гимастатин. У этих бактерий есть фермент, который может соединить два мономера на самом последнем этапе синтеза, превращая каждый из атомов углерода, которые необходимо соединить, в высокореакционноспособные радикалы.
Чтобы имитировать этот процесс, исследователи сначала создали сложные мономеры из строительных блоков аминокислот с помощью технологии быстрого синтеза пептидов, ранее разработанной в лаборатории Пентелуте.
«Используя твердофазный пептидный синтез, мы могли быстро пройти через многие этапы синтеза и легко смешивать и сочетать строительные блоки», — говорит Д’Анджело. «Это лишь один из способов, которым наше сотрудничество с Pentelute Lab было очень полезным».
Затем исследователи использовали новую стратегию димеризации, разработанную в лаборатории Мовассаги, чтобы соединить вместе две сложные молекулы. Эта новая димеризация основана на окислении анилина с образованием углеродных радикалов в каждой молекуле. Эти радикалы могут реагировать с образованием углерод-углеродной связи, которая связывает два мономера вместе. Используя этот подход, исследователи могут создавать димеры, содержащие различные типы субъединиц, в дополнение к встречающимся в природе димерам гимастатина.
«Причина, по которой мы были в восторге от этого типа димеризации, заключается в том, что он позволяет вам действительно разнообразить структуру и очень быстро получить доступ к другим потенциальным производным», — говорит Мовассаги.
Разрушение мембраны
Один из вариантов, созданных исследователями, имеет флуоресцентную метку, которую они использовали для визуализации того, как гимастатин взаимодействует с бактериальными клетками. Используя эти флуоресцентные зонды, исследователи обнаружили, что лекарство накапливается в мембранах бактериальных клеток. Это привело их к гипотезе о том, что он работает, разрушая клеточную мембрану, что также является механизмом, используемым по крайней мере одним одобренным FDA антибиотиком, даптомицином.
Исследователи также разработали несколько других вариантов гимастатина, заменив разные атомы в определенных частях молекулы, и протестировали их противомикробную активность в отношении шести бактериальных штаммов. Они обнаружили, что некоторые из этих соединений обладали высокой активностью, но только если они включали один встречающийся в природе мономер вместе с другим.
- «Соединяя вместе две полные половины молекулы, мы могли получить производное гимастатина только с одной флуоресцентной меткой. Только с этой версией мы могли проводить микроскопические исследования, которые свидетельствовали о локализации гимастатина в бактериальных мембранах, потому что симметричные версии с двумя метками не обладали нужной активностью», — говорит Д’Анджело.
- Эндрю Майерс, профессор химии Гарвардского университета, говорит, что новый синтез включает в себя «захватывающие новые химические инновации».
- «Этот подход позволяет проводить окислительную димеризацию полностью синтетических мономерных субъединиц для получения антибиотика гимастатина способом, связанным с его биосинтезом», — говорит Майерс, не участвовавший в исследовании. «Путем синтеза ряда аналогов были выявлены важные взаимосвязи структура-активность, а также доказательства того, что натуральный продукт функционирует на уровне бактериальной оболочки».
Теперь исследователи планируют разработать больше вариантов, которые, как они надеются, могут иметь более мощную антибиотическую активность.
«Мы уже определили позиции, которые мы можем дериватизировать, которые потенциально могут либо сохранить, либо усилить активность. Что действительно интересно для нас, так это то, что значительное количество производных, к которым мы получили доступ в процессе разработки, сохраняют свою противомикробную активность», — говорит Мовассаги.
Исследование финансировалось Национальным институтом здравоохранения, Канадским советом по естественным наукам и инженерным исследованиям и стипендией для выпускников Национального научного фонда.
Метки: Антибиотики
- Превращение пластикового мусора в химическое сокровище
- Истинный механизм аммиачного катализа
- Катализатор, превращающий воду в энергетическое богатство
- Жидкие металлы меняют процессы химического машиностроения
- Влияние электричества на химический синтез
- Прорыв в области электрокатализаторов для производства H2O2
- Раскрытие атомных тайн распада металла
- Преобразование сельского хозяйства с помощью микробных удобрений
- Уничтожение прочных пластиковых соединений
- Возрождения метода Барбье с помощью механохимией
