Получение. Свойства
Физические свойства. При обычных условиях первые два члена ряда (С3 — С4) — газы, (С5 — С16) — жидкости, начиная с C17 — твердые вещества. Температуры кипения и плавления циклоалканов выше, чем у соответствующих алканов.
Получение.
1. Основной способ получения циклоалканов — отщепление двух атомов галогена от дигалогеналканов:
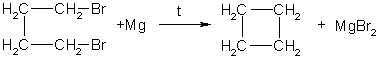
2. При каталитическом гидрировании ароматических углеводородов образуются циклогексан или его производные:
t°,P,Ni
C6H6 + 3H2 → C6H12.
Химические свойства. По химическим свойствам малые и обычные циклы существенно различаются между собою. Циклопропан и циклобутан склонны к реакциям присоединения, т.е. сходны в этом отношении с алкенами. Циклопентан и циклогексан по своему химическому поведению близки к алканам, так как вступают в реакции замещения.
1. Так, например, циклопропан и циклобутан способны присоединять бром (хотя реакция и идет труднее, чем с пропеном или бутеном):
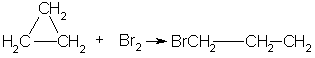
2. Циклопропан, циклобутан и даже циклопентан могут присоединять водород, давая соответствующие нормальные алканы.
Присоединение происходит при нагревании в присутствии никелевого катализатора:
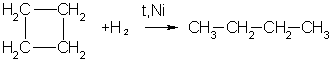
3. В реакцию присоединения с галогеноводородами опять же вступают только малые циклы. Присоединение к гомологам циклопропана происходит по правилу Марковникова:
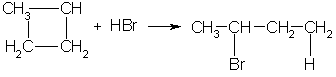
4. Реакции замещения. Обычные циклы (С6 и выше) устойчивы и вступают только в реакции радикального замещения подобно алканам:
t°
С6Н12 + Вr2 → С6Н11Вr + НВr.
5. Дегидрирование циклогексана в присутствии никелевого катализатора приводит к образованию бензола:
t° Ni
C6H12 → C6H6 + 3H2.
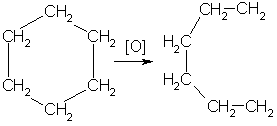
6. При действии сильных окислителей (например, 50%-ной азотной кислоты) на циклогексан в присутствии катализатора образуется адипиновая (гександиовая) кислота:
Особенности строения циклоалканов и их химическое поведение. Выше мы продемонстрировали неустойчивость малых циклов и их способность разрываться и вступать в реакции присоединения. Причины этого кроются в строении циклов. Так, циклопропан имеет плоское строение, поэтому атомы водорода у соседних атомов углерода располагаются над и под плоскостью цикла в энергетически невыгодном ("заслоненном") положении. Это — одна из причин "напряженности" цикла и его неустойчивости.
Исходя из того, что трехчленный цикл является плоским равносторонним треугольником, валентные углы между атомами углерода должны быть равными 60°, т.е. резко отличающимися от величины нормального валентного утла 109,5° для классического случая sp‘-гибридизации 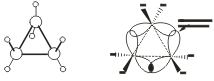 .
.
Установлено, что образование s-связей между атомами углерода происходит путем перекрывания sp3-гибридных орбиталей не по прямой, соединяющей ядра атомов, а вне ее.
Такое перекрывание не является осевым, характерным для образования s-связей, а несколько приближается к боковому перекрыванию, характерному для образования p-связей. Образовавшиеся s-связи с расположением максимальной электронной плотности вне прямой между ядрами связываемых атомов называют "банановыми". По свойствам они напоминают p-связи. Действительно, циклопропан способен вступать в реакции присоединения (с разрывом цикла).
Обычные циклы, наоборот, очень устойчивы и не склонны к разрыву. Так, молекула циклогексана не является плоским многоугольником и принимает различные конформации.
Среди неплоских конформаций наиболее энергетически выгодной является конформация кресла, так как в ней все валентные углы между атомами углерода равны 109,5°, а атомы водорода у соседних атомов углерода находятся относительно друг друга в заторможенном положении.
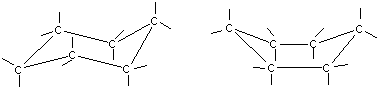
a б
Конформации шестичленного цикла: а — кресло: 6 — ванна.
Другое возможное для циклогексана расположение атомов соответствует конформации ванны, хотя оно менее устойчиво, чем конформация кресла. Следует отметить, что и в конформации кресла, и в конформации ванны связи вокруг каждого атома углерода имеют тетраэдрическое расположение. Отсюда — несравнимо большая устойчивость обычных циклов по сравнению с малыми циклами, отсюда — их возможность вступать в реакции замещения, но не присоединения.
